細胞のメカニカルストレス感知メカニズム解明に貢献

この度、2022年にJournal of Biomechanical Science and Engineering(Vol.17 No.3)に掲載された機械工学科の片岡則之教授(写真右)、小熊靖之准教授、機械工学専攻博士後期課程の岡知輝さん(写真左)の論文が、Papers of the Year Award 2022に選出され、6月3日に行われた日本機械学会第35回バイオエンジニアリング講演会にて表彰されました。掲載された論文『Real-time analysis of F-actin fluctuation in living cells with quasi super-resolution technique』は、疑似超解像度画像解析手法を用いて生細胞内細胞骨格の実時間観察を試みた結果をまとめたもので、細胞プロセスのメカニズム解明に寄与するものとして期待されています。
片岡教授の喜びの声とともに、研究について詳しくお話を伺いました。
―Papers of the Year Award 2022 の受賞、おめでとうございます。感想をお聞かせください。
 率直に言って大変嬉しいです。Journal of Biomechanical Science and Engineeringは日本機械学会の英文誌の1つで、バイオエンジニアリング部門のオフィシャルジャーナルであるとともに、Asian-Pacific Association for Biomechanicsのオフィシャルジャーナルにもなっている国際的な雑誌です。現在はアジア太平洋地域の投稿論文も多くなっており、エディターも半分以上が海外の方です。そうした全投稿論文の中から、その年の最優秀論文として選出されるPapers of the Year Awardを受賞したことは、大変意義深いことだと思っています。工学部機械工学科の生体工学研究は今、国内の拠点になりつつあります。事実、工学部のホームページを見て、ここで生体工学を研究したいと希望して来た中国からの留学生もいます。特に新型コロナウイルス対策に関する研究において、生体工学という領域が世界的にも着目されている時です。
率直に言って大変嬉しいです。Journal of Biomechanical Science and Engineeringは日本機械学会の英文誌の1つで、バイオエンジニアリング部門のオフィシャルジャーナルであるとともに、Asian-Pacific Association for Biomechanicsのオフィシャルジャーナルにもなっている国際的な雑誌です。現在はアジア太平洋地域の投稿論文も多くなっており、エディターも半分以上が海外の方です。そうした全投稿論文の中から、その年の最優秀論文として選出されるPapers of the Year Awardを受賞したことは、大変意義深いことだと思っています。工学部機械工学科の生体工学研究は今、国内の拠点になりつつあります。事実、工学部のホームページを見て、ここで生体工学を研究したいと希望して来た中国からの留学生もいます。特に新型コロナウイルス対策に関する研究において、生体工学という領域が世界的にも着目されている時です。
それだけではなく、様々な病気の原因解明や治療法に関する研究に生体工学が大きく関わっており、我々も注力していますが、癌に関する研究が盛んに行われています。今回の受賞をきっかけに、日本のみならず海外に向けて生体工学の拠点の一つとして工学部の存在をアピールしていきたいと考えています。
―論文の内容について、詳しく説明いただけますか。
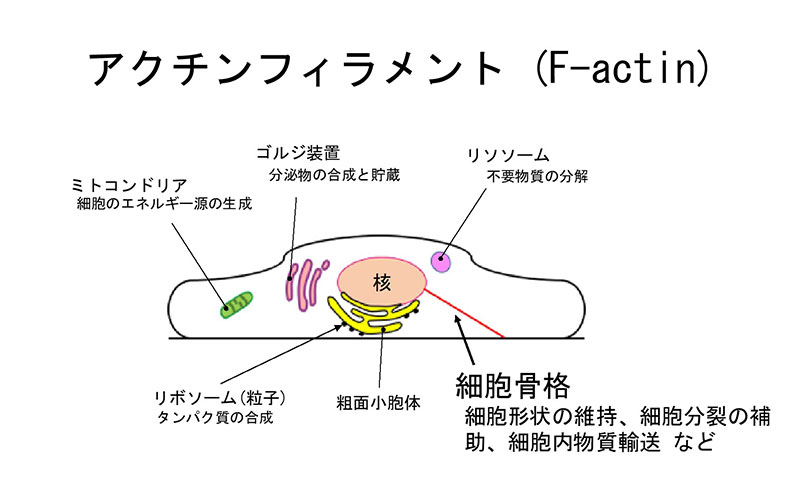 細胞内には様々な器官がありますが、その一つにアクチンフィラメント(以下、F-アクチン)があります。1本が6~7ナノメーターの繊維成分で構成されるF-アクチンは、筋肉の収縮、細胞の運動性、小胞および細胞小器官の運動、細胞シグナル伝達、細胞の機械的感知機構など、多くの細胞プロセスにおいて重要な役割を果たしています。しかし、細胞の力学刺激に対する感知機構については、未解明な事柄も多いのです。これら細胞プロセスのメカニズムを解明するには、細胞内の F-アクチン構造リモデリングを観察することが重要です。
細胞内には様々な器官がありますが、その一つにアクチンフィラメント(以下、F-アクチン)があります。1本が6~7ナノメーターの繊維成分で構成されるF-アクチンは、筋肉の収縮、細胞の運動性、小胞および細胞小器官の運動、細胞シグナル伝達、細胞の機械的感知機構など、多くの細胞プロセスにおいて重要な役割を果たしています。しかし、細胞の力学刺激に対する感知機構については、未解明な事柄も多いのです。これら細胞プロセスのメカニズムを解明するには、細胞内の F-アクチン構造リモデリングを観察することが重要です。
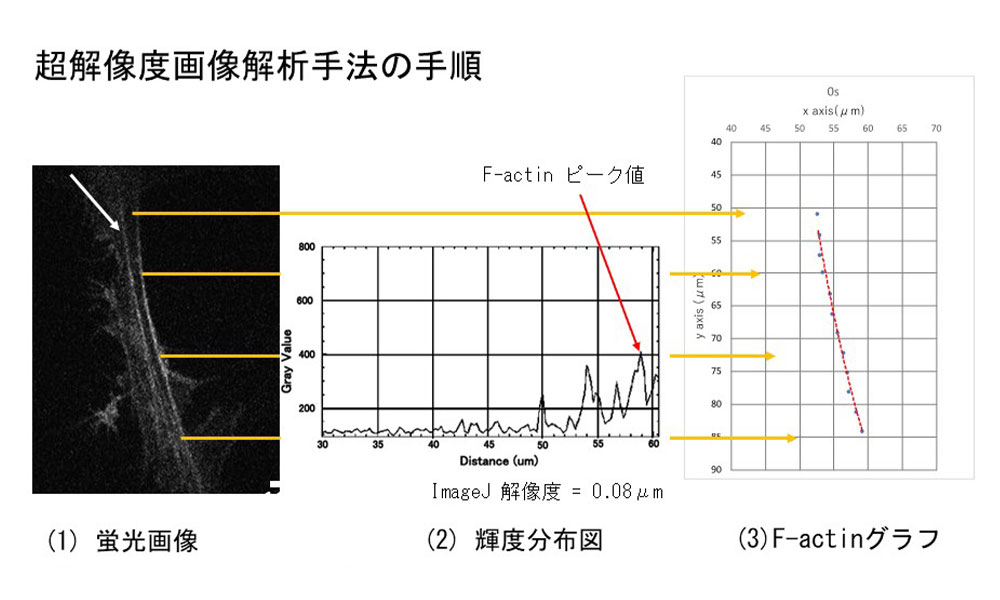
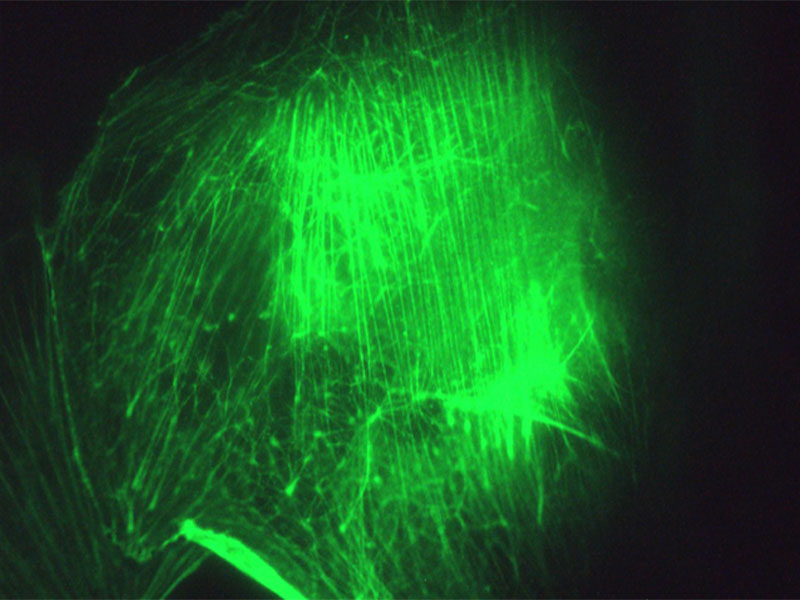 私たちは熱によるF-アクチンの微小変動に着目し、これまで静的な構造体として観察されてきたF-アクチンを動的な構造体として解析する手法を確立しました。初めに蛍光顕微鏡で観察した際の計測結果では、F-アクチンのゆらぎの振幅は約0.2~0.3μmでした。これは光学分解能とほぼ同じで、観察の限界に近い値であり信頼性のないデータとなります。そこで、擬似超解像技術を用いて断面蛍光プロファイルから細胞内のF-アクチン画像を再構成しました。
私たちは熱によるF-アクチンの微小変動に着目し、これまで静的な構造体として観察されてきたF-アクチンを動的な構造体として解析する手法を確立しました。初めに蛍光顕微鏡で観察した際の計測結果では、F-アクチンのゆらぎの振幅は約0.2~0.3μmでした。これは光学分解能とほぼ同じで、観察の限界に近い値であり信頼性のないデータとなります。そこで、擬似超解像技術を用いて断面蛍光プロファイルから細胞内のF-アクチン画像を再構成しました。
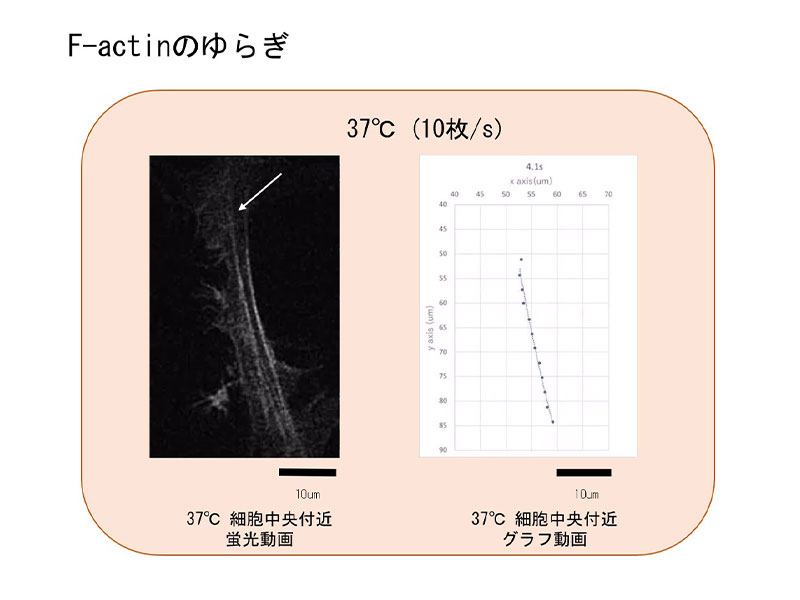
蛍光輝度分布の中の輝度のピーク値にF-アクチンが存在すると仮定して、1本のフィラメントに対して10本のピーク値の座標を取得。解析の結果、蛍光画像ではぼんやりと揺らいでいるように見えたものが、10秒間に0.3μmほど揺らいでいることが明確になりました。さらに、この擬似超解像度画像解析手法によって、空間分解能(位置的に接近した2点を独立した2点として見分ける能力)を2.5倍ほど改善することができました。
―どのような点が評価されたと思われますか。
一つは、細胞プロセスのメカニズムの解明につながる成果として評価されたと思います。さらに、ハードウェアではなくソフトウェア、すなわち高額な装置を使うのではなく、自ら考えた手法を使って解析した点が評価されたのではないかと考えています。工学というとモノづくりやデバイス開発など、実用化に直結した分野に見られがちですが、バイオエンジニアリングは理学的なサイエンスにウエイトを置いており、基礎的な研究も多い分野です。
 我々の研究の特徴でもありますが、細胞プロセスのメカニズムといった未知の現象解明に工学技術を応用しています。細胞の微小な振動を捉え、解像度を上げるなどの工夫とアイデアにより超解像度画像解析を可能にしました。この技術はバイオに留まらず、例えば監視カメラなど詳細な画像解析を必要とする様々な分野に応用することができます。基礎研究から生まれる工学技術は応用範囲が広く、工学から理学を見て、また理学から工学に応用できるのが、この研究の魅力とも言えます。
我々の研究の特徴でもありますが、細胞プロセスのメカニズムといった未知の現象解明に工学技術を応用しています。細胞の微小な振動を捉え、解像度を上げるなどの工夫とアイデアにより超解像度画像解析を可能にしました。この技術はバイオに留まらず、例えば監視カメラなど詳細な画像解析を必要とする様々な分野に応用することができます。基礎研究から生まれる工学技術は応用範囲が広く、工学から理学を見て、また理学から工学に応用できるのが、この研究の魅力とも言えます。
―今後の目標についてお聞かせください。
本論文では画像処理の手法を開発しましたが、これを使って細胞全体の力学刺激に対する感知メカニズムについて解析していきます。流れや引張りなど、常に人間の体の中の全ての細胞が力学刺激を受けていますが、どのように感知してるのかは、未だ明らかにされていません。このメカニズムが分かれば、いろいろな病気の解明や診断治療にも応用できます。現在、医学部と共同で、DFAT (dedifferentiated fat cell : 脱分化脂肪細胞)を使った再生医療への応用に向けた研究を進めています。細胞の力学刺激の感知メカニズムを知ることにより、再生医療に大いに役立つとともに、様々な分野への応用が期待できます。

―ありがとうございました。今後益々のご活躍を祈念しております。
★Journal of Biomechanical Science and Engineering(Vol.17 No.3)はこちら
★マイクロバイオエンジニアリング研究室はこちら










